Regulatory Affairs Manager (m/w/d)
Für diese Stelle werden keine Bewerbungen mehr angenommen.
Ihr Aufgabenbereich bei uns
- Als Regulatory Affairs Manager sind sie innerhalb des Unternehmens für die erfolgreiche Zulassung neuer Produkte verantwortlich.
- Dazu organisieren sie alle Maßnahmen, die nötig sind, um von nationalen und internationalen Behörden die Genehmigung für Entwicklung, Herstellung, Vermarktung und Vertrieb der Produkte zu erhalten (USA, Japan, Kanada, Australien, Europa, Brasilien).
- Sie dafür zuständig, die Sicherheit, Qualität und Wirksamkeit von unseren Produkten gegen- über verschiedenen internationalen Zulassungsbehörden nachzuweisen und zu zeigen, dass die nationalen und internationalen Vorschriften, Verfahrensrichtlinien und Grundsätze berücksichtigt werden.
- Als Regulatory Affairs Manager betreuen Sie Produkte über die gesamte „Lebenszeit“ hinweg.
- Sie koordinieren dabei die Arbeit der einzelnen Abteilungen (z.B. mit Entwicklung, Produktion, Qualiätssicherung, etc.), die mit dem Produkt zu tun haben, fügen ihre Ergebnisse zusammen, haben Freude am Umgang mit rechtlichen Fragestellungen und arbeiten auf den erfolgreichen Zulassungsantrag hin.
Das zeichnet Sie aus
- Sie besitzen ein abgeschlossenes, technisches Fach-/Hochschulstudium im Bereich Qualitätsmanagement / Medizintechnik oder eine vergleichbare Ausbildung.
- Alternativ besitzen Sie eine andere Qualifikation, mit der Sie uns überzeugen können.
- Idealerweise bereits Berufserfahrung in der Medizintechnik bzw. im Umgang mit Zulassungen.
- Sie besitzen eine Affinität für die Auseinandersetzung mit rechtlichen und regulatorischen Anforderungen für Medizinprodukte.
- Sie bringen eine selbstständige, sorgfältige und lösungsorientierte Arbeitsweise mit.
- Sie haben keine Scheu Verantwortung zu übernehmen und sind sind engagiert, neue Prozessse zu entwickeln und einzuführen.
- Es ist kein Problem für Sie, gewisse Projekte (mündlich und schriftlich) in Englisch abzuwickeln.
Das bieten wir Ihnen
- Seit der Gründung im Jahr 2011 haben uns wir uns vom MedTech Start-Up zum etablierten Unternehmen entwickelt. Wir haben noch großes vor und Sie können diese Reise mitgestalten.
- Wir sind ein agiles Unternehmen – d.h. Sie können Ihre Ideen sofort einbringen und bei vielen wichtigen Entscheidungen mitwirken.
- Ihre Fähigkeiten können Sie bei einer äußerst abwechslungsreichen und verantwortungsvollen Tätigkeit einsetzen.
- Sie möchten sich weiterbilden? Wir sind offen für alle weiterführenden internen- und externen Schulungen.
- Sie planen langfristig? Sehr gut, wir auch – d.h. der Arbeitsvertrag ist unbefristet.
- Ihr Engagement wird attraktiv und leistungsgerecht vergütet.
- Wir bieten ein flexibles Arbeitszeitmodell.
- Sie können sich bei 30 Tagen Urlaub im Jahr ausruhen.
Stellenanzeige als PDF
Über evonos
evonos entwickelt und fertigt hochwertige neurochirurgische Instrumente, Implantate und OP-Leuchten, die von führenden Chirurg*innen weltweit genutzt werden.
Die Wahl unserer Produkte ist jedoch nicht nur in deren Qualität begründet, sondern auch in unserem Wissen über den chirurgischen Prozess und die Bedürfnisse derjenigen, die im Operationssaal tätig sind.
An unserem Standort in Tuttlingen arbeiten wir deshalb bereits seit zehn Jahren verantwortungsbewusst und unermüdlich an jedem Detail, das den Komfort für Anwender wie auch für Patienten steigert.
Wir freuen uns über Ihre aussagekräftige Bewerbung inklusive Eintrittstermin und Gehaltsvorstellung an: jobs@evonos.de
evonos GmbH & Co. KG | Herr Ingolf Diez | Stockacher Str. 134 | 78532 Tuttlingen


 evoDrill
evoDrill evoFix
evoFix evoFix Steril
evoFix Steril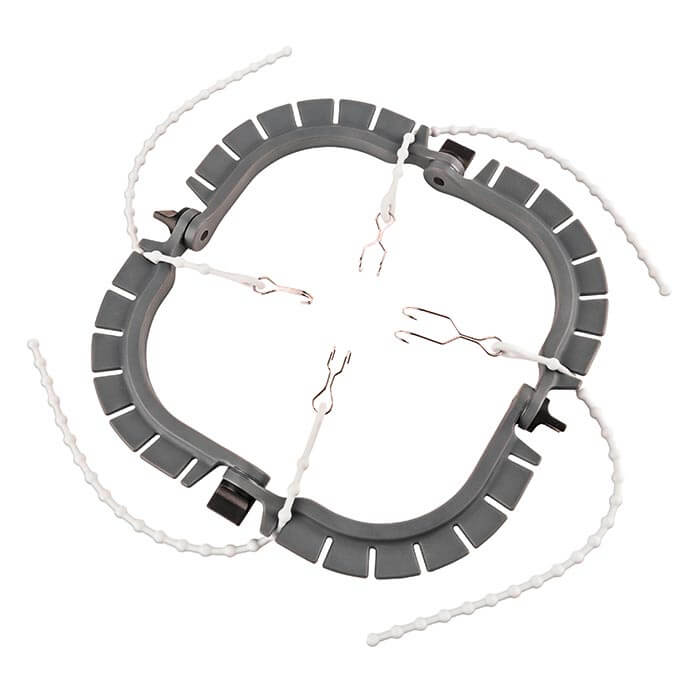 evoFrame
evoFrame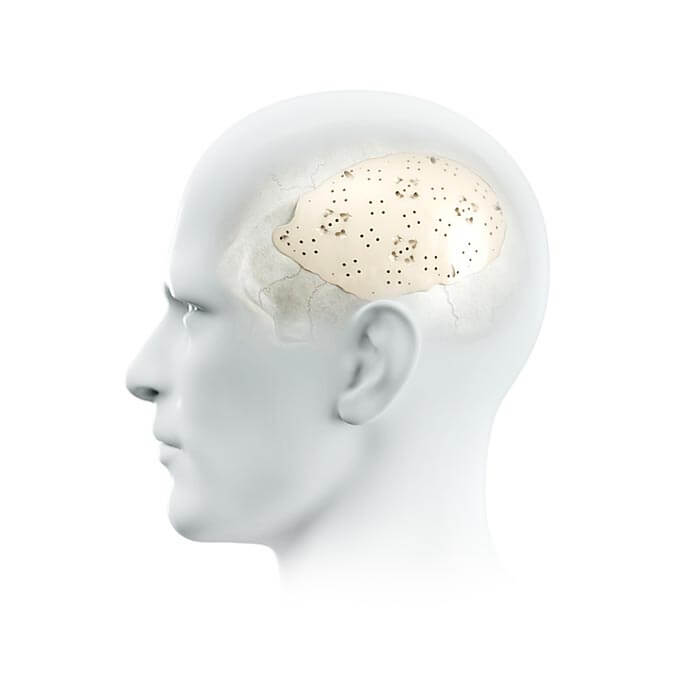 evoShape
evoShape evoLight
evoLight evoBase
evoBase evoClip
evoClip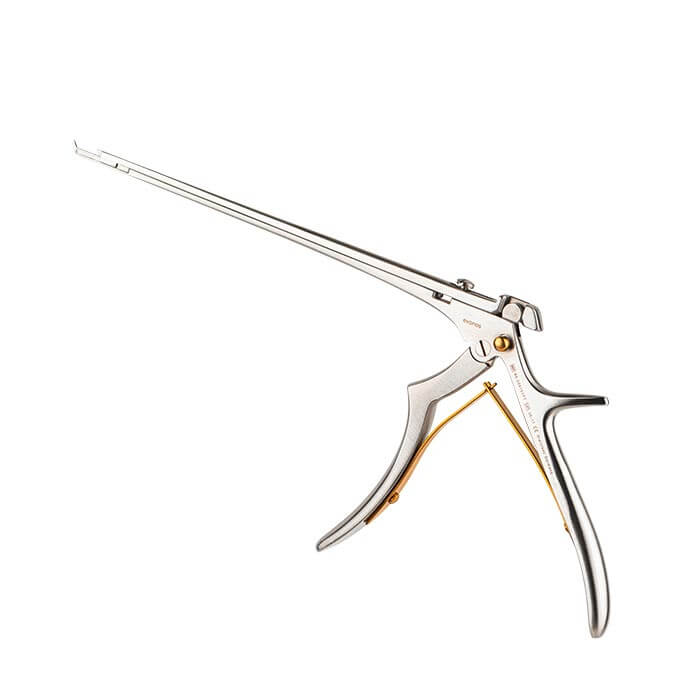 evoBite
evoBite evoCarat
evoCarat